
IMUNIZAÇÃO
Municípios do RS recebem vacinas contra Covid-19 a partir desta terça-feira
A distribuição começa nesta terça-feira, de acordo com as solicitações e o levantamento dos municípios do Rio Grande do Sul.

IMUNIZAÇÃO
A distribuição começa nesta terça-feira, de acordo com as solicitações e o levantamento dos municípios do Rio Grande do Sul.
Notícia
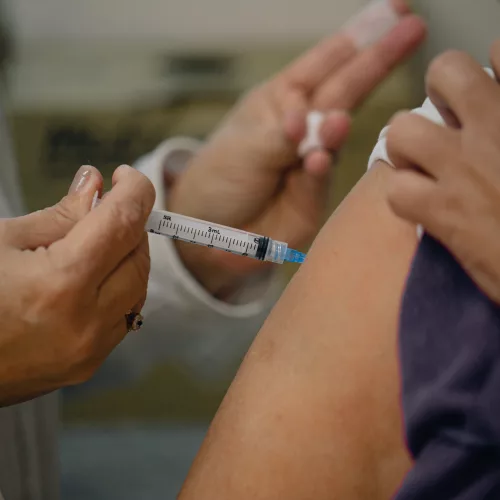
O objetivo da dose de reforço é ampliar a coberturas vacinal da população mais propensa a desenvolver formas graves da Covid-19
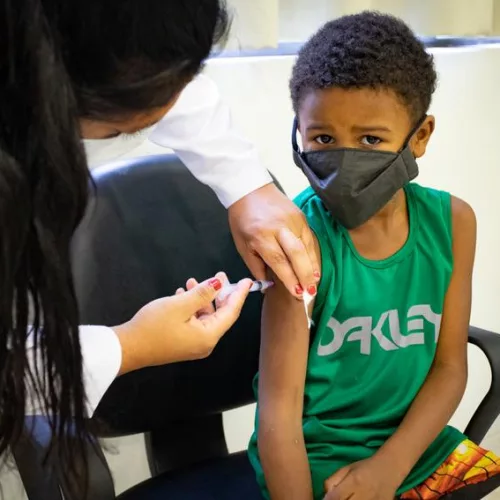
CAMPANHA DE VACINAÇÃO
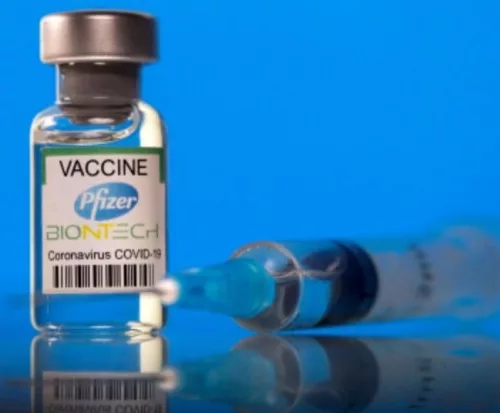
O Ministério da Saúde recomenda que a dose seja feita com a vacina pediátrica da Pfizer.
Notícia
Para identificação, os frascos das vacinas bivalentes têm tampa na cor cinza, cada um com seis doses.

Brasil e Mundo
A vacina para crianças de 6 meses a 4 anos de idade tem dosagem e composição diferentes.

Redes Sociais
Em relação à pólio, o reforço nos pontos de vacinação é necessário devido à campanha nacional de combate à doença.
Brasil e Mundo
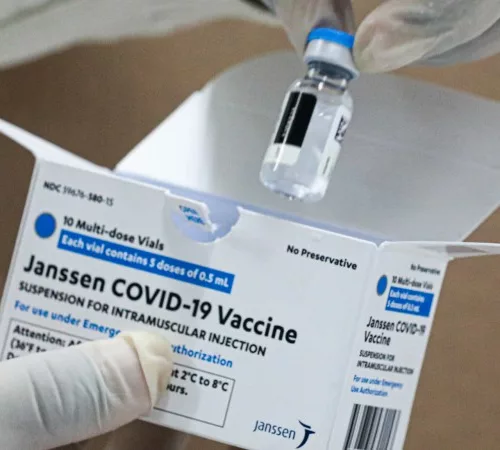
Segundo o Ministério da Saúde, a vacina deve ser aplicada quatro vezes.

Redes Sociais
Também houve uma atualização para quem fez o esquema primário com a vacina da Janssen.
Brasil e Mundo
A eficácia e a segurança da vacina CoronaVac para crianças de 3 a 5 anos foram debatidas, nesta terça-feira (22), entre técnicos da Anvisa e especialistas em saúde.

Brasil e Mundo
Os pesquisadores afirmam que as próximas semanas serão fundamentais para entender a dinâmica de transmissão da doença no Brasil.

Redes Sociais
Se todas essas que estão em atraso já tivessem feito a dose, a porcentagem da população gaúcha com dose de reforço passaria dos atuais 31% para 53%.

Brasil e Mundo
Fabricado em parceria com a AstraZeneca, a vacina será entregue ao Ministério da Saúde para ser incluído no Programa Nacional de Imunizações.
Redes Sociais
A SES (Secretaria Estadual da Saúde) destinará todas as vacinas contra a Covid-19 da Coronavac que estejam em estoque no Rio Grande do Sul para a aplicação imediata em crianças de seis a 11 anos, utilizando-as como primeira dose. Segundo a secretária da Saúde, Arita Bergmann, a ação significa a disponibilidade de 605 mil doses, […]

Brasil e Mundo
O ministro da Saúde também respondeu que os testes “irão chegar”. Segundo Queiroga, até fevereiro serão distribuídos mais 40 milhões de testes para estados.

Brasil e Mundo
A vacina CoronaVac é a mesma utilizada atualmente na imunização de adultos, sem nenhum tipo de adaptação para uma versão pediátrica.